Theoretisch super, praktisch nicht
Photokathoden aus Kupferoxid: Laserexperiment deckt Ursachen für hohe Verluste auf.
Kupferoxid könnte in Solarzellen oder als Photokathode für die solare Energieumwandlung theoretisch hohe Wirkungsgrade ermöglichen. Praktisch aber kommt es zu großen Verlusten. Nun konnte ein Team am HZB mit einem raffinierten Femtosekunden-Laserexperiment aufklären, wo diese Verluste stattfinden: Sie treten weniger an den Grenzflächen auf, sondern vielmehr bereits im Innern des kristallinen Materials. Diese Ergebnisse geben Hinweise, um Kupferoxid und andere Metalloxide für Anwendungen als Energiematerialien zu optimieren.
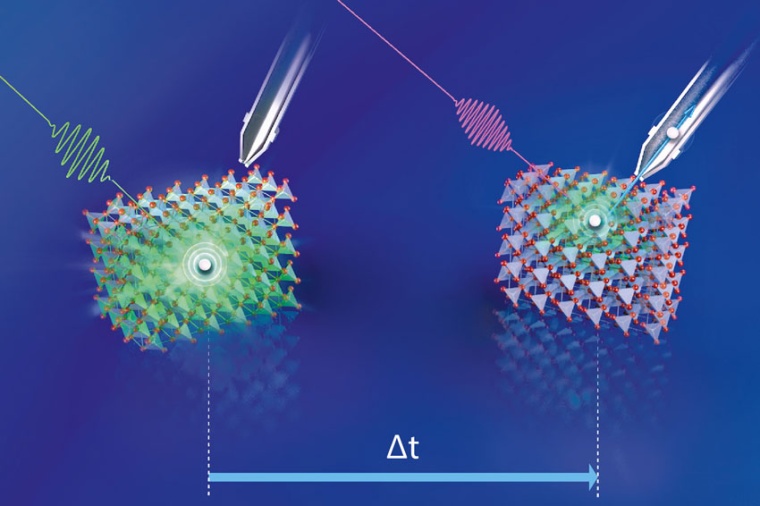
Kupferoxid ist ein aussichtsreicher Kandidat für die zukünftige solare Energieumwandlung: Als Photokathode könnte der Halbleiter Kupferoxid mit Sonnenlicht Wasser elektrolytisch aufspalten und so den Brennstoff Wasserstoff erzeugen, der die Energie des Sonnenlichts chemisch speichert.
Einkristallines Kupferoxid besitzt eine Bandlücke von 2 eV, die sehr gut zum solaren Energiespektrum passt. Perfekte Kupferoxid-Kristalle sollten unter Lichtbestrahlung theoretisch eine Spannung nahe 1,5 Volt bereitstellen. Damit wäre das Material sehr gut geeignet als Top-Absorber in einer Stapelzelle für die solare Wasserspaltung und sollte einen Wirkungsgrad von Sonnenenergie zu chemischer Energie in Wasserstoff von bis zu 18 Prozent ermöglichen. Doch die realen Werte für die Photospannung liegen deutlich darunter und reichen nicht aus, um Kupferoxid effizient als Photokathode in einer Stapelzelle für die solare Wasserspaltung zu verwenden. Bisher wurden vor allem Verlustprozesse nahe der Oberfläche bzw. an Grenzschichten dafür verantwortlich gemacht.
Nun hat ein Team am HZB-Institut für Solare Brennstoffe diese Prozesse unter die Lupe genommen. Sie erhielten hochwertige Cu2O-Einkristalle von des California Institute of Technology und bedampften sie zusätzlich mit einer hauchdünnen, transparenten Schicht aus Platin. Diese Platinschicht fungiert als Katalysator und steigert die Effizienz der Wasseraufspaltung. Sie untersuchten diese Proben im Femtosekunden-Laserlabor am HZB, um herauszufinden, welche Prozesse zum Verlust der Ladungsträger führen und insbesondere auch, ob diese Verluste im Innern der Einkristalle auftreten oder an der Grenzfläche zum Platin.
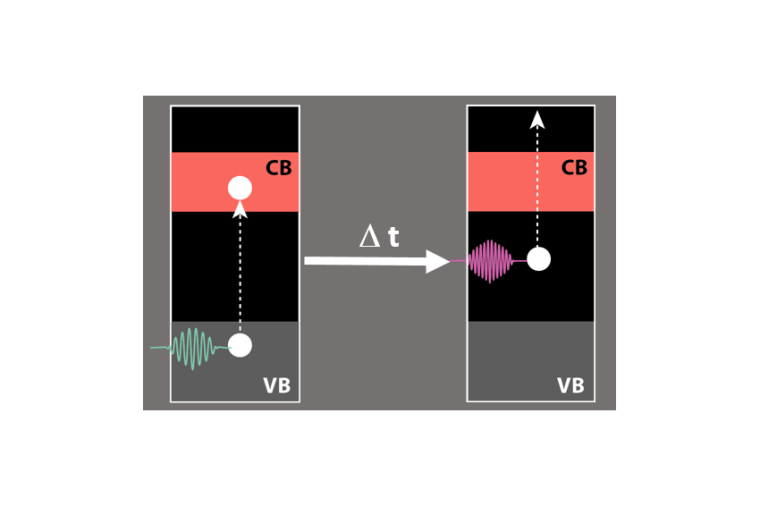
Dafür regte ein erster Laserpuls im sichtbaren grünen Bereich die Elektronen im Cu2O an; nur Bruchteile von Sekunden später folgte ein zweiter Laserpuls (UV-Licht), um die Energie des angeregten Elektrons zu messen. Mit dieser zeitaufgelösten Zwei-Photonen-Photoemissions-Spektroskopie (tr-2PPE) konnten sie den Hauptmechanismus von Photospannungsverlusten identifizieren. „Wir beobachteten, dass die angeregten Elektronen sehr schnell in Defektzuständen gebunden werden, die in der Bandlücke selbst in großer Zahl existieren“, berichtet Erstautor Mario Borgwardt, der inzwischen seine Arbeit als Humboldt-Stipendiat am Lawrence Berkeley National Laboratory in den USA fortsetzt. Der Koordinator der Studie Dennis Friedrich führt aus: „Dies geschieht auf einer Zeitskala von unter einer Pikosekunde, also extrem schnell, vor allem im Vergleich zu der Zeit, in der Ladungen aus dem Inneren des kristallinen Materials an die Oberfläche diffundieren können.“
„Wir haben am Femtosekunden-Laserlabor des HZB sehr leistungsstarke experimentelle Methoden, um Energie und Dynamik von photoangeregten Elektronen in Halbleitern zu analysieren. Für Kupferoxid konnten wir zeigen, dass die Verluste kaum an den Grenzflächen zum Platin auftreten, sondern im Kristall selbst“, sagt der Initiator der Studie und Leiter der Femtosekunden-Spektroskopie am HZB, Rainer Eichberger.
„Mit diesen neuen Einblicken liefern wir einen ersten Beitrag zum Exzellenzcluster UniSysCat der TU Berlin, an dem wir beteiligt sind“, betont Roel van de Krol, der das HZB-Institut für Solare Brennstoffe leitet. In UniSysCat stehen katalytische Prozesse im Fokus, die auf sehr unterschiedlichen Zeitskalen stattfinden: Während Ladungsträger auf Anregungen durch Licht extrem schnell reagieren – Femtosekunden bis Pikosekunden –, benötigen chemische Prozesse wie die Katalyse viele Größenordnungen mehr Zeit. Für eine erfolgreiche Photokatalyse müssen jedoch beide Prozesse gemeinsam optimiert werden. Die vorliegenden Ergebnisse sind ein wichtiger Schritt auf diesem Weg.
HZB / od
Weitere Infos
- Originalveröffentlichung
M. Borgwardt et al.: Femtosecond time-resolved two-photon photoemission studies of ultrafast carrier relaxation in Cu2O photoelectrodes, Nat. Comm.; DOI: 10.1038/s41467-019-10143-x - Institut für solare Brennstoffe, Helmholtz-Zentrum Berlin für Materialien und Energie GmbH, Berlin
Meist gelesen

Salzige Kruste auf dem Roten Planeten
Daten des Marsmaulwurfs zeichnen komplexes Bild der obersten Gesteinsschichten auf unserem Nachbarplaneten.

Quantenkopplung von Licht und Schall
Neue, effiziente Methode verschränkt Photonen mit akustischen Phononen.

Neue Einblicke in die Struktur von Atomkernen
Präzisionsmessungen setzen Grenzen für die Stärke einer möglichen dunklen Kraft zwischen Neutronen und Elektronen.
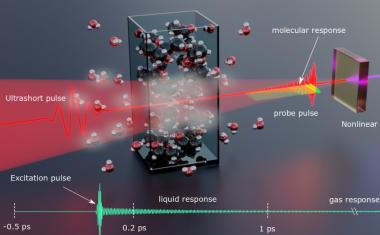
Moleküle klar identifizieren
Femtosekunden-Feldoskopie im nahen Infrarot kann winzige Flüssigkeitsmengen messen.

Vermutung aus der Stringtheorie bewiesen
Mathematisches Problem im Zusammanhang mit der Vier-Gravitonen-Streuung gelöst.







