Rekonstruktion der Sauerstoffbildung auf der Erde
Erkenntnisse können auch für die Produktion von grünem Wasserstoff bedeutsam sein.
Der molekulare Sauerstoff der Erdatmosphäre wird durch die lichtgetriebene Spaltung von Wasser in Pflanzen, Algen und Cyanobakterien gebildet. Diesen Prozess konnten Forscher jetzt in aufwändigen Experimenten mit Infrarotlicht nachverfolgt und mittels quantenchemischer Simulationen nachzuverfolgen. Die Studie des Teams um Physiker der FU Berlin und der Universität L’Aquila in Italien liefert Einblicke in den biologischen Prozess, der wahrscheinlich in den letzten drei Milliarden Jahren auf der Erde unverändert abgelaufen ist. Die Wissenschaftler betonen auch den Zusammenhang zur Produktion von grünem Wasserstoff oder anderen erneuerbaren Brennstoffen, die dem biologischen Vorbild folgt. „In technischen Systemen zur Produktion erneuerbarer Brennstoffe sind sowohl die Verwendung seltener Edelmetalle als auch hohe Energieverluste ein Problem. Nun können gezielt edelmetallfreie Materialien entwickelt werden, bei denen die gekoppelte Bewegung der Elektronen und Protonen minimale Energieverluste ermöglicht", sagt Holger Dau von der FU Berlin.
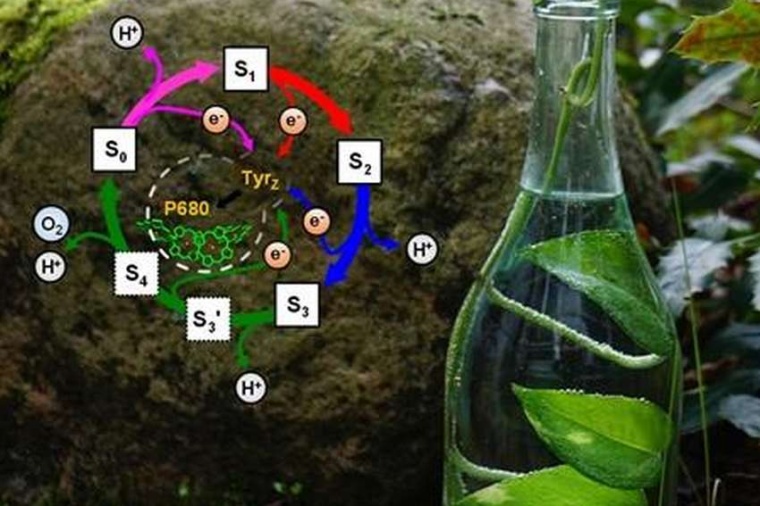
Die Photosynthese liefert die Energie für das Leben auf der Erde, indem sie Sonnenenergie in chemischer Form speichert. In der Photosynthese sowie auch in technischen Systemen für eine nachhaltige Treib- und Brennstoffproduktion ist die Wasserspaltung eine zentrale Reaktion, mittels der mobile Elektronen und Protonen aus dem Rohstoff Wasser gewonnen werden können und molekularer Sauerstoff freigesetzt wird. Die heutige sauerstoffreiche Atmosphäre der Erde resultiert aus der photosynthetischen O2-Produktion während der Wasserspaltung am proteingebundenen Mangan-Cluster des Photosystems II der Pflanzen, Algen und Cyanobakterien.
Die Bildung des O2-Moleküls beginnt in einem Zustand mit vier angesammelten Elektronenlöchern, dem S4-Zustand, der vor mehr als einem halben Jahrhundert postuliert wurde und seitdem rätselhaft geblieben ist. Die Forscher konnten jetzt diese fehlende Schlüsselelement in der photosynthetischen O2-Bildung identifizieren. Nach mehrjähriger Vorbereitung gelang ein aufwändiges Experiment, mit dem die Bewegungen der Elektronen und Protonen verfolgt werden konnten. Hierzu wurden Partikel des Photosystem II-Chlorophyll-Protein-Komplexes aus vierzig Kilogramm Spinat isoliert. Dann wurden über sieben Monate etwa drei Millionen Laserblitze gefeuert und für jeden von diesen der Zeitverlauf eines Infrarotsignals mit Mikrosekundenzeitauflösung aufgezeichnet.
Mehrere Terabyte an Messdaten wurden anschließend analysiert und ergaben in Kombination mit Molekülmechanik-Berechnungen für fast 600.000 Atome und quantenchemischen Simulationen das folgende Bild: Zunächst wird im Protein eine entscheidende Protonenleerstelle durch elektrostatisch ferngesteuerte Seitenkettendeprotonierung erzeugt. Anschließend wird in einem erstaunlichen Einzelelektronen-Multiprotonen-Transferereignis ein reaktives Sauerstoffradikal gebildet. Das ist der langsamste Schritt in der photosynthetischen O2-Bildung mit nur moderater Energiebarriere und überraschender entropischer Verlangsamung. Die Forscher identifizieren somit den zuvor rätselhaften S4-Zustand als ein Sauerstoffradikalzustand. Auf seine Bildung folgen eine schnelle O-O-Bindung und O2-Freisetzung.
In Verbindung mit früheren Durchbrüchen bei experimentellen und rechnerischen Untersuchungen ergibt sich nun ein überzeugendes atomistisches Bild der photosynthetischen O2-Bildung, wie die Wissenschaftler betonen. Die Studie liefert somit einen Einblick in einen biologischen Prozess, der wahrscheinlich seit drei Milliarden Jahren auf die gleiche einzigartige Weise von statten gegangen ist, wodurch auch das wissensbasierte Design künstlicher Wasserspaltungssysteme unterstützen wird.
FU Berlin / RK
Weitere Infos
- Originalveröffentlichung
P. Greife et al.: The electron–proton bottleneck of photosynthetic oxygen evolution, Nature, online 3. Mai 2023; DOI: 10.1038/s41586-023-06008-5 - Biophysik und Photosynthese (H. Dau), FB Physik, Frei Universität Berlin
- Dept. of Information Engineering, Computer Science and Mathematics, University of L’Aquila, Italien